Kiel vi apartigas alkoholon de akvo?
Elektu taŭgan grandecon kaj formon por via dezirata planto kaj alkoholoj havas similajn ecojn ĉar akvo molekuloj enhavas hidroksilgrupojn kiuj povas formi hidrogenajn ligojn kun aliaj akvo molekuloj kaj kun alkoholo molekuloj, kaj same alkoholo molekuloj povas formi hidrogenajn ligojn kun aliaj alkoholo molekuloj same kiel kun akvo.
Apartigo de alkoholo de akvo
Apartigi miksaĵon de alkoholo (etanolo) kaj akvo, vi povas uzi procezon konata kiel frakcia distilado. Ĉi tiu tekniko dependas de la fakto, ke la komponaĵoj en la miksaĵo havas malsamajn bolpunktojn. Ĉar etanolo bolas je pli malalta temperaturo (78.5 celsiaj gradoj, aŭ 173.3 gradoj Fahrenheit) ol akvo, la alkoholo vaporiĝas dum la plej granda parto de la akvo restas likva. Bona distila kolono produktos miksaĵon de 95 procento da alkoholo kaj 5 procento de akvo. Ĉi tiu proporcio reprezentas la plej puran formon de etanolo ebla kun distilado kaj estas vaste akceptita kiel industria normo.
- Verŝu la miksaĵon de etanolo/akvo en la rondfundan flakon.
- Kunvenu la frakcian distilaparaton alkroĉante la frakcian kolumnon al la rondmalsupra flakono. Aligu la kondensilon al la frakcia kolumno kaj metu la distila-kaptan flakon sub ĝi por kapti la distilon..
- Metu la Bunsen-brulilon sub la rondfundan flakon kaj varmigu la miksaĵon super la bolpunkto de etanolo. (pri 80 gradoj C).
- Konservu la miksaĵon je konstanta temperaturo ĝis la bolado ĉesos. Nun, vi finis distiladon.
Kio estas Frakcia Distilado
Frakcia distilado estas la procezo de apartigo de substanco en ĝiajn partojn (aŭ frakcioj), profitante malsamajn vaporpremajn ecojn de tiuj substancoj. Frakcia distilado estas ofte uzata kiel sinonimo kun "distilado" ĉar distilado ĉiam utiligas diferencon en bolpunktoj de komponentsubstancoj por apartigo..
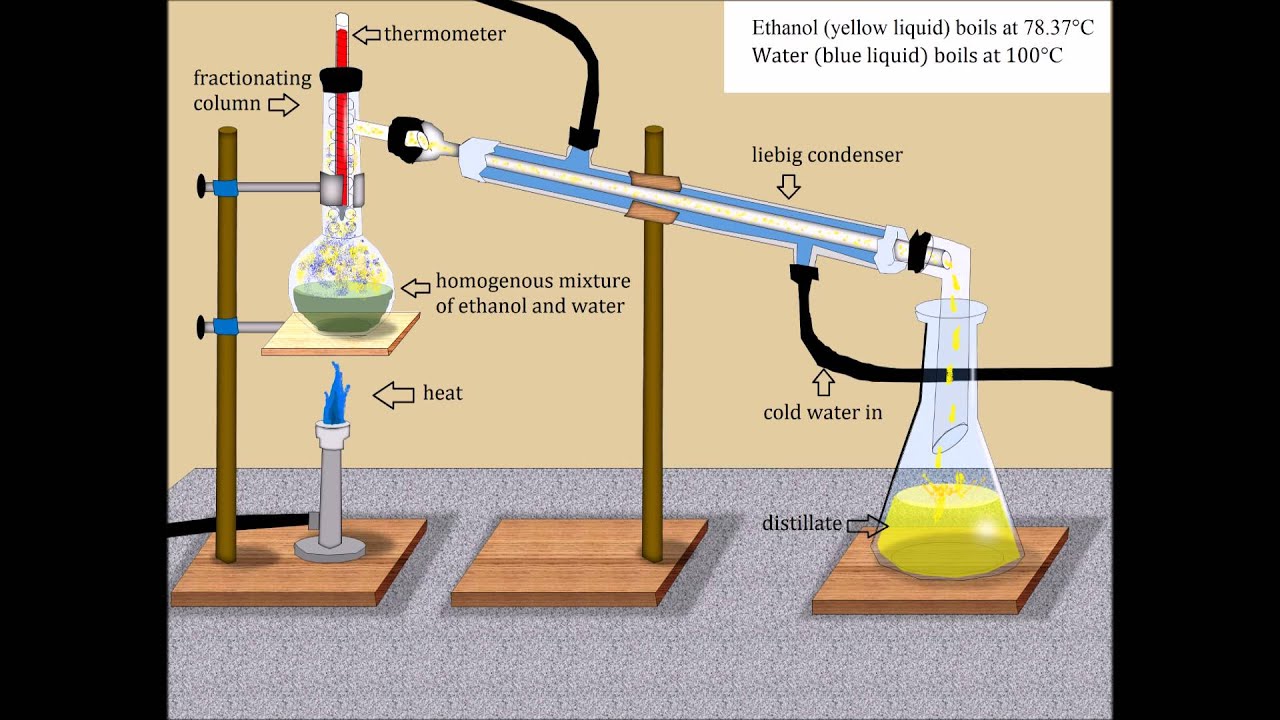
frakcia distilado de alkoholo kaj akvo
La bazaj paŝoj al distilado estas:
- Aldonu varmon al likva miksaĵo kun du aŭ pli da ĉefaj substancoj; ekzemple, miksaĵo de akvo kaj etanolo.
- Dum la likvaĵo varmiĝas, komponantoj kun la pli malaltaj bolpunktoj komencos vaporiĝi kaj leviĝu tra la kolono. En la ekzemplo de akvo/etanol, etanolo forbolos unue (BP 78°C, kompare kun akvo (BP 100°C). Tamen, la vaporo leviĝanta ankoraŭ enhavos kelkajn molekulojn de la aliaj substancoj. Vaporo fariĝas pli pura ju pli alte ĝi altiĝas en la kolono, ĉar pli pezaj molekuloj "falas" kaj revenas al likvaĵo.
- Ĉar vaporo pliiĝas en la distila kolono, pli pezaj molekuloj kondensos reen en likvaĵon kaj "pluvo" reen malsupren. En iu ajn punkto en frakciiga kolumno, vaporo leviĝos, likvaĵo falos, kaj molekuloj miksiĝos. Kolumnoj nature havas certajn "stadiojn"; stadio estas areo en la kolono kun simila kvanto da molekuloj de ĉiu speco de substanco (t.e. ĝenerala certa procento de akvo kaj etanolo). Kolumnoj estas dizajnitaj por esti sufiĉe altaj por atingi certan procentan apartigon, per trovado de la minimuma nombro da bezonataj stadioj.
- Vaporo atingas la supron de la kolono (distilo) estas kolektita en industrian kondensilon (granda malvarmigilo), kiu malvarmigas la vaporon reen en likvaĵon, kaj tubigita al tanko aŭ stokado.
- Substancoj restantaj en la kolono daŭrigas la procezon de distilado, ĝis la dezirata pureco estas atingita. Kelkaj kolumnoj estas kontinua procezo (la mezo), kie nova bazsolvo estas daŭre aldonita. Aliaj estas bataj sistemoj, kie la bazo estas forigita kiam dezirata apartigo estas atingita. En multaj sistemoj, solvo estas recirkulata plurajn fojojn por certigi, ke substancoj estas konvene apartigitaj.
Kio estas priskribita supre estas la baza procezo de distilado. Distiladkolono foje estas referita kiel frakcieca distilkolono en industrio. Kolumnoj kiuj nur disigas du substancojn povas esti nomitaj frakciantaj kolumnoj. Frakcia distilsistemo kutime atingas pluraj malsamaj produktoj ĉe multoblaj punktoj ene de la kolono. Dum substancoj altiĝas, miksaĵoj povas esti tiritaj en diversaj stadioj, kaj kondensita.
Kredito:
https://www.epicmodularprocess.com/blog/fractional-distillation


Lasu respondon
Vi devas Ensaluti aŭ registri aldoni novan respondon.