แยกแอลกอฮอล์กับน้ำยังไง
น้ำ และ แอลกอฮอล์ มีคุณสมบัติคล้ายกันเพราะว่า น้ำ โมเลกุลประกอบด้วยหมู่ไฮดรอกซิลที่สามารถสร้างพันธะไฮโดรเจนกับกลุ่มอื่นได้ น้ำ โมเลกุลและด้วย แอลกอฮอล์ โมเลกุล, และเช่นเดียวกัน แอลกอฮอล์ โมเลกุลสามารถสร้างพันธะไฮโดรเจนกับโมเลกุลอื่นได้ แอลกอฮอล์ โมเลกุลอีกด้วย น้ำ.
การแยกแอลกอฮอล์ออกจากน้ำ
เพื่อแยกส่วนผสมแอลกอฮอล์ (เอทานอล) และน้ำ, คุณสามารถใช้กระบวนการที่เรียกว่าการกลั่นแบบเศษส่วนได้. เทคนิคนี้ขึ้นอยู่กับข้อเท็จจริงที่ว่าสารประกอบในส่วนผสมมีจุดเดือดต่างกัน. เนื่องจากเอทานอลเดือดที่อุณหภูมิต่ำกว่า (78.5 องศาเซลเซียส, หรือ 173.3 องศาฟาเรนไฮต์) กว่าน้ำ, แอลกอฮอล์จะระเหยไปในขณะที่น้ำส่วนใหญ่ยังคงเป็นของเหลว. คอลัมน์การกลั่นที่ดีจะทำให้เกิดส่วนผสมของ 95 เปอร์เซ็นต์แอลกอฮอล์และ 5 เปอร์เซ็นต์น้ำ. อัตราส่วนนี้แสดงถึงรูปแบบเอธานอลที่บริสุทธิ์มากที่สุดเท่าที่จะเป็นไปได้ด้วยการกลั่น และได้รับการยอมรับอย่างกว้างขวางว่าเป็นมาตรฐานอุตสาหกรรม.
- เทส่วนผสมเอทานอล/น้ำลงในขวดก้นกลม.
- ประกอบเครื่องกลั่นแบบแยกส่วนโดยติดเสาแยกส่วนเข้ากับขวดก้นกลม. ติดคอนเดนเซอร์เข้ากับคอลัมน์การแยกส่วน และวางขวดสำหรับจับกลั่นไว้ข้างใต้เพื่อจับสารกลั่น.
- วางหัวเผาแผดเผาไว้ใต้ขวดก้นกลม และตั้งความร้อนส่วนผสมให้อยู่เหนือจุดเดือดของเอธานอล (เกี่ยวกับ 80 องศาเซลเซียส).
- รักษาส่วนผสมไว้ที่อุณหภูมิคงที่จนกว่าการเดือดจะหยุดลง. มะเร็งท่อนำไข่, คุณทำการกลั่นเสร็จแล้ว.
การกลั่นแบบเศษส่วนคืออะไร
การกลั่นแบบเศษส่วนเป็นกระบวนการแยกสารออกเป็นส่วนต่างๆ (หรือเศษส่วน), โดยใช้ประโยชน์จากคุณสมบัติความดันไอต่างๆ ของสารเหล่านั้น. การกลั่นแบบเศษส่วนมักใช้เป็นคำพ้องความหมายกับ "การกลั่น" เนื่องจากการกลั่นมักจะใช้ประโยชน์จากจุดเดือดที่แตกต่างกันของส่วนประกอบต่างๆ เพื่อแยกสาร.
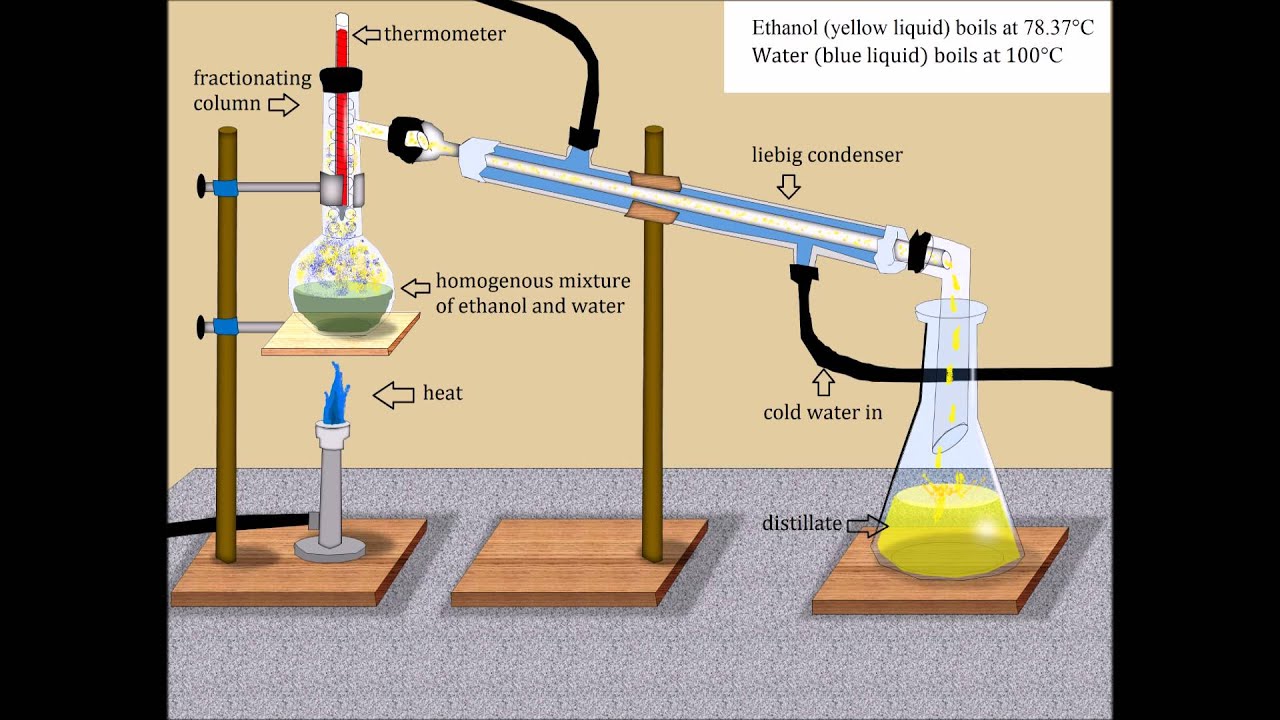
การกลั่นแอลกอฮอล์และน้ำแบบเศษส่วน
ขั้นตอนพื้นฐานในการกลั่นคือ:
- เพิ่มความร้อนให้กับส่วนผสมของเหลว ที่มีสารหลักตั้งแต่ 2 ชนิดขึ้นไป; ตัวอย่างเช่น, ส่วนผสมของน้ำและเอธานอล.
- ขณะที่ของเหลวร้อนขึ้น, ส่วนประกอบที่มีจุดเดือดต่ำกว่าจะเริ่มระเหย และลุกขึ้นผ่านเสา. ในตัวอย่างน้ำ/เอธานอล, เอธานอลจะเดือดก่อน (ความดันโลหิต 78° C, เมื่อเทียบกับน้ำ (ความดันโลหิต 100°C). อย่างไรก็ตาม, ไอที่เพิ่มขึ้นจะยังคงประกอบด้วยโมเลกุลของสารอื่นอยู่บ้าง. ไอจะบริสุทธิ์มากขึ้นตามปริมาณที่เพิ่มขึ้นในคอลัมน์, เมื่อโมเลกุลที่หนักกว่า "หลุดออก" และเปลี่ยนกลับเป็นของเหลว.
- เมื่อไอระเหยเพิ่มขึ้นในคอลัมน์การกลั่น, โมเลกุลที่หนักกว่าจะควบแน่นกลับเป็นของเหลวและ "ฝน" กลับลงมา. ณ จุดใดจุดหนึ่งในคอลัมน์การแยกส่วน, ไอจะเพิ่มขึ้น, ของเหลวจะตก, และโมเลกุลจะผสมกัน. คอลัมน์จะมี "ขั้นตอน" บางอย่างโดยธรรมชาติ; ระยะคือพื้นที่ในคอลัมน์ที่มีจำนวนโมเลกุลเท่ากันของสารแต่ละชนิด (เช่น. เปอร์เซ็นต์น้ำและเอทานอลโดยทั่วไป). คอลัมน์ได้รับการออกแบบให้สูงพอที่จะทำให้มีการแยกเปอร์เซ็นต์ได้, โดยการหาจำนวนขั้นขั้นต่ำที่ต้องการ.
- ไอระเหยไปถึงด้านบนของคอลัมน์ (กลั่น) ถูกรวบรวมไว้ในคอนเดนเซอร์อุตสาหกรรม (เครื่องทำความเย็นขนาดใหญ่), ซึ่งทำให้ไอระเหยกลับกลายเป็นของเหลว, และต่อท่อไปยังถังหรือถังเก็บ.
- สารที่เหลืออยู่ในคอลัมน์จะดำเนินกระบวนการกลั่นต่อ, จนกว่าจะถึงความบริสุทธิ์ที่ต้องการ. บางคอลัมน์เป็นกระบวนการต่อเนื่อง (ที่พบมากที่สุด), โดยมีการเพิ่มโซลูชั่นพื้นฐานใหม่อย่างต่อเนื่อง. อื่นๆ เป็นระบบแบตช์, โดยที่ฐานจะถูกลบออกเมื่อได้การแยกที่ต้องการ. ในหลายระบบ, สารละลายจะถูกหมุนเวียนซ้ำหลายครั้งเพื่อให้แน่ใจว่าสารต่างๆ ถูกแยกออกจากกันอย่างเหมาะสม.
สิ่งที่อธิบายไว้ข้างต้นคือกระบวนการกลั่นขั้นพื้นฐาน. คอลัมน์การกลั่นบางครั้งเรียกว่าคอลัมน์การกลั่นแบบเศษส่วนในอุตสาหกรรม. คอลัมน์ที่แยกสารสองตัวเท่านั้นสามารถเรียกว่าคอลัมน์การแยกส่วน. ระบบการกลั่นแบบแยกส่วนมักจะประสบความสำเร็จ ผลิตภัณฑ์ที่แตกต่างกันหลายอย่าง ที่ หลายจุด ภายในคอลัมน์. เมื่อสารเพิ่มขึ้น, ส่วนผสมสามารถดึงออกได้ในขั้นตอนต่างๆ, และควบแน่น.
เครดิต:
https://www.epicmodularprocess.com/blog/fractional-distillation


ทิ้งคำตอบไว้
คุณต้อง เข้าสู่ระบบ หรือ ลงทะเบียน เพื่อเพิ่มคำตอบใหม่.