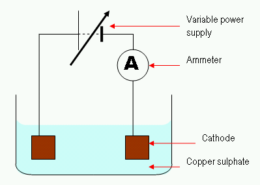
电解铜为什么会放出铜 (二) 硫酸盐溶液?
题
在里面 铜的电解 (二) 硫酸盐溶液, 铜离子的排出量与铜量成正比 (二) 溶解在溶液中的离子. 通过各种过程从溶液中去除释放的离子, 包括被固体物质吸收或溶解在水中.
铜质 (二) 硫酸盐溶液, 铜离子与阴离子结合 (硫酸盐) 在氧化还原反应中. 总的反应是:
2铜(小号) + 3H2O (升) -> 2铜离子 (水) + 2SO4(水)
SO4 离子还原后释放出铜离子, 这导致氢气的形成.
电解铜时铜的放电 (二) 硫酸盐溶液产生的原因如下:
1. CuSO的溶解 4 在水中释放出 Cu2+ 离子. 这些离子与水分子的电子结合形成 H2O2. 第二个反应是放热反应并释放热量, 导致铜的放电.
2. CuSO4的解离 4 分解为 Cu 和 SO 4 2- 离子还释放 Cu2+ 和 SO4+. 这些离子与水分子的电子结合形成 H2O 和 HSO4-. 最终结果是这些盐的浓度增加,而 CuSO4 的浓度减少 4 .


离开一个答案
你必须 登录 要么 寄存器 添加新答案.