Forskjellen mellom hydrogenbinding og metallbinding
Hva er Hydrogen Bond?
Hydrogenbinding er en form for intermolekylær kraft som oppstår når hydrogen bindes med svært elektronegative elementer som nitrogen, oksygen eller fluor. I et slikt molekyl, det negativt ladede atomet har en delvis negativ ladning, og hydrogen har en delvis positiv ladning. De relativt ladede delene av molekylene tiltrekker hverandre sterkt, som polene til magnetene.
Hva er Metallic Bond?
Metallisk binding oppstår mellom atomer i et metall. De ytterste elektronene i metallatomene blir løsnet eller “delokalisert.” På dette tidspunktet tilhører de delokaliserte elektronene ikke noe spesielt atom, men deles som et fellesskap “elektronbasseng.” De positivt ladde kjernene til atomene er alle tiltrukket av disse elektronene, som holder et metallstykke sammen.
Forskjeller mellom metallisk og hydrogenbinding
Metallisk Bond
Metaller er preget av lyse, glans, høy elektrisk og termisk ledningsevne, formbarhet, duktilitet og høy strekkfasthet. En metallisk krystall består av et veldig stort antall atomer arrangert i et regelmessig mønster. Ulike modeller har blitt foreslått for å forklare naturen til metallisk binding, de to viktigste modulene er som følger:
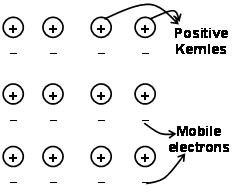
Kreftene som holder atomene sammen i et metall som et resultat av tiltrekningen mellom positive ioner og omkringliggende fritt bevegelige elektroner er kjent som metallbindinger.
Gjennom elektronhavet predated kvantemekanikk forklarer det fortsatt på tilfredsstillende måte visse egenskaper til metallene. Den elektriske og termiske ledningsevnen til metaller for eksempel, kan forklares med tilstedeværelsen av mobile elektroner i metaller. Om å påføre et elektronfelt, disse mobile elektronene leder elektrisitet gjennom metallene fra en ende til en annen. på samme måte, hvis en del av metall er oppvarmet, de mobile elektronene i den delen av metallene får en stor mengde kinetisk energi. Å være gratis og mobil, disse elektronene beveger seg raskt gjennom metallet og leder varme til den andre delen av metallet.
Betingelser for Metallic Bond
Metallbinding kan beskrives som å dele frie elektroner mellom positivt ladede metallioniske gitter. Strukturen til metallbindingen er veldig forskjellig fra strukturen til den kovalente bindingen og den ioniske bindingen. I metallbindingen, valenselektronene delokaliserer S- og p-orbitalene fra de interagerende metallatomene. Det er, de kretser ikke rundt sine respektive metallatomer, men rundt de positivt ladede kjernene til de interagerende metallionene for å danne”hav” av elektroner. Da beveger elektronene seg fritt i rommet mellom atomkjernene.
Nøkler dannes vanligvis fordi individuelle atomer er ustabile og bindingsdannelse skaper en mer stabil struktur.
Alle atomer har valenselektroner: antall grupper i det periodiske systemet forteller deg hvor mange valenselektroner som har et bestemt grunnstoff eller metall (dette skiller seg fra d-blokkelementet, dvs. overgangsmetallet).
Typer metallisk binding
Metaller er mer flytende, men egentlig ikke bundet på krystallinsk måte. Salesforce-sertifisert. Noen flytende elektroner rundt de nært tilknyttede atomene. Tre tilstander av materie eksisterer.
Krystall- regelmessig ordnet rekke av atomer/molekyler- nødvendig for strukturbestemmelse gjennom røntgenkrystalografi
Væske-dvs. Flytting av enheter i umiddelbar nærhet ( Jeg kan ta feil, men måten det ble forklart for meg på er at "solid" ikke er en tilstand av materie. Metaller er nærmere liguider. Noen væsker har delvis, ufullstendige bindinger som er i flyt dvs. Vann Metallisk binding. Jeg snakker egentlig bare om pgf 1 av denne wiki-artikkelen. hvis du leser artikkelen, det blir komplisert. Tilsynelatende metaller selv om faste stoffer er nærmere væsker enn Chrystals og selvfølgelig gasser.
Gass- ytterligere spredte enheter, dvs. Molekyler/atomer
Viktigheten av Metallic Bond
Metalliske bindinger la elementene lede elektrisitet, de kan formes til former og de leder varme lett. Dette er den sterkeste av de tre store obligasjoner fordi elektronene er delt i mer enn bare de første skallene. Jo flere skjell er involvert i å dele elektroner, jo sterkere knytte bånd.
Hydrogenbinding
Et hydrogenatom koblet kovalent til et sterkt elektronegativt atom kan etablere en ekstra svak binding til et annet elektronegativt atom i samme eller forskjellige molekyler. Denne tilknytningen kalles en hydrogenbinding. For å skille fra en normal kovalent binding, en hydrogenbinding er representert med en stiplet linje, f.eks. X – H…Y hvor X & Y er to elektronegative atomer. Styrken på hydrogenbindingen er ganske lav ca 2-10 kcal mol-1 eller 8,4–42 kJ mol-1 sammenlignet med en kovalent bindingsstyrke 50–100 kcal mol-1 eller 209 -419 kJ ganger-1
Betingelser for hydrogenbinding
Hydrogen bør være knyttet til et svært elektronegativt element.
Størrelsen på det elektronegative elementet må være liten.
Disse to kriteriene er oppfylt av F, DE, og N i det periodiske systemet. Større elektronegativitet og mindre størrelse, jo sterkere er hydrogenbindingen som er tydelig fra den relative rekkefølgen av energier til hydrogenbindinger.
Typer hydrogenbinding
Intermolekylær hydrogenbinding:Denne typen binding finner sted mellom to molekyler av samme eller forskjellige typer. For eksempel,
Intermolekylær hydrogenbinding fører til molekylær assosiasjon i væsker som vann etc. I vann ser det altså ut til at bare noen få prosent av vannmolekylene ikke er hydrogenbundet selv ved 90°C. Å bryte disse hydrogenbindingene gjennom hele væsken krever betydelig varmeenergi. Dette er indikert i de relativt høyere kokepunktene til hydrogenbundne væsker. Krystallinsk hydrogenfluorid består av polymeren (HF)n. Dette har en sikk-sakk-kjedestruktur som involverer
H-binding.
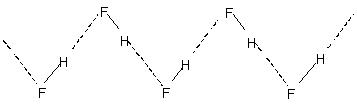
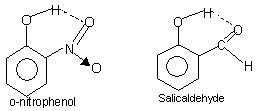
Intramolekylær hydrogenbinding: Denne typen binding skjer mellom atomer av samme molekyl som er tilstede på forskjellige steder. Intramolekylær hydrogenbinding gir opphav til en lukket ringstruktur som begrepet chelering noen ganger brukes for. Eksempler er
o-nitrofenol, salisylaldehyd.
Viktigheten av hydrogenbinding i biologiske systemer
Hydrogenbinding spiller en viktig rolle i fysiologiske systemer. Proteiner inneholder kjeder av aminosyrer. Aminosyreenhetene er ordnet i en spiralform noe som en strukket spiralfjær (danner en helix). N-H-gruppen til hver aminosyreenhet og den fjerde C=O-gruppen som følger den langs kjeden, etablerer N–H—O hydrogenbindinger. Disse bindingene er delvis ansvarlige for stabiliteten til spiralstrukturen. Dobbelhelixstrukturen til DNA består også av to tråder som danner en dobbelhelix og er forbundet med hverandre gjennom hydrogenbinding.
Effekt av hydrogenbinding
Hydrogenbinding har hatt en veldig uttalt effekt på visse egenskaper til molekylene. De har fått effekter på
- Stoffets tilstand
- Løselighet av stoffet
- Kokepunkt
- Surhet av forskjellige isomerer
Disse kan fremgå av de følgende eksemplene.
Forskjellen er at. H2O er en væske ved vanlig temperatur mens H2S er en gass selv om både O og S tilhører samme gruppe i det periodiske systemet.
Løsning: H2O er i stand til å danne intermolekylære hydrogenbindinger. Dette er mulig på grunn av høy elektronegativitet og liten størrelse på oksygen. På grunn av intermolekylær H-binding, molekylær assosiasjon finner sted. Som et resultat øker den effektive molekylvekten og dermed øker kokepunktet. Så H2O er en væske. Men i H2S ingen hydrogenbinding er mulig på grunn av stor størrelse og mindre elektronegativitet av S. Så dets kokepunkt er lik kokepunktet til en isolert H2S-molekylet og derfor er det en gass.
Forskjellen er at.Etyl alkohol (C2H5ÅH) har et høyere kokepunkt enn dimetyleter (CH3-BARE O3) selv om molekylvekten til begge er lik.
Løsning: Selv om etylalkohol og dimetyleter har samme molekylvekt, men i etylalkohol danner hydrogenet i OH-gruppene intermolekylær hydrogenbinding med OH-gruppen i et annet molekyl. Men i tilfelle eter er hydrogenet koblet til C er ikke så elektronegativt at det oppmuntrer hydrogenet til å komme fra hydrogenbinding.
På grunn av intermolekylær H-binding, etylalkohol forblir i tilhørende form og koker derfor ved høyere temperatur sammenlignet med dimetyleter.
Kreditt:https://www.askiitians.com/iit-jee-chemical-bonding/metallic-and-hydrogen-bonding.html


Legg igjen et svar
Du må Logg Inn eller registrere for å legge til et nytt svar.